Aufgabe 1
Bei der Reaktion von Eisen mit Schwefel kann man unter
verschiedenartigen Reaktionsbedingungen entweder Eisensulfid oder
Pyrit erhalten.
Eisensulfid ist durch folgendes Massenverhältnis
charakterisiert: m(Fe):m(S) = 1,74.
Pyrit ist durch folgendes Massenverhältnis charakterisiert:
m(Fe):m(S) = 0,871.
Stelle die Verhältnisformeln für Eisensulfid und Pyrit
auf!
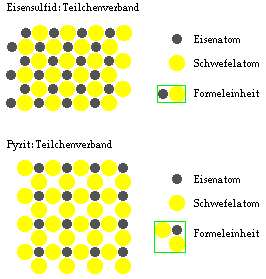
Stelle auf der Basis des Teilchenmodells der Materie eine
Stoffportion Eisensulfid und eine Stoffportion Pyrit dar!
(ma(Fe) = 55,847 u; ma(S) = 32,066 u).
Lösung:
A. Eisensulfid
Die Elemente Eisen und Schwefel stehen in folgendem
Massenverhältnis:
m(Fe):m(S) = 1,74:1
Oder anders angeschrieben:
m(Fe) 1,74 ----- = ---- (1) m(S) 1
Nimmt man - unter Berücksichtigung des Teilchenmodells - an, dass:
a. die Eisenportion der Masse m(Fe) aus x Eisenatomen der Masse ma (Fe) besteht, dann folgt:
m(Fe) = x * ma(Fe)
b. die Schwefelportion der Masse m(S) aus y Schwefelatomen der Masse ma(S) besteht, dann folgt:
m(S) = y * ma(S)
Durch Einsetzen in (1) erhält man:
x * ma(Fe) 1,74 ----------- = ---- y * ma(S) 1
Durch Einsetzen der Massen ma(Fe) = 55,847 u und ma(S) = 32,066 u erhält man:
x * 55,847 u 1,74 ------------- = ---- y * 32,066 u 1
Durch Umsetzen erhält man:
x 1,74 * 32,066 u - = ---------------- y 55,847 u
Durch Vereinfachen und Ausrechnen erhält man:
x 1 - = - y 1
Da x die Anzahl der Eisenatome angibt und y die Anzahl der Schwefelatome, kennt man nun das Anzahlverhältnis der Atome in Eisensulfid:
N(Fe):N(S) = 1:1 auf ein Eisenatom kommt ein Schwefelatom
Die Verhältnisformel für Eisensulfid gibt dieses Anzahlverhältnis an. Folglich lautet die Verhältnisformel für Eisensulfid:
FeS N(Fe):N(S) = 1:1
B. Pyrit
Die Elemente Eisen und Schwefel stehen in folgendem
Massenverhältnis:
m(Fe):m(S) = 0,871:1
Oder anders angeschrieben:
m(Fe) 0,871 ----- = ----- (2) m(S) 1
Nimmt man - unter Berücksichtigung des Teilchenmodells - an, dass:
a. die Eisenportion der Masse m(Fe) aus x Eisenatomen der Masse ma(Fe) besteht, dann folgt:
m(Fe) = x * ma(Fe)
b. die Schwefelportion der Masse m(S) aus y Schwefelatomen der Masse ma(S) besteht, dann folgt:
m(S) = y * ma(S)
Durch Einsetzen in (2) erhält man:
x * ma(Fe) 0,871 ----------- = ----- y * ma(S) 1
Durch Einsetzen der Massen ma(Fe) = 55,847 u und ma(S) = 32,066 u erhält man:
x * 55,847 u 0,871 ------------- = ----- y * 32,066 u 1
Durch Umsetzen erhält man:
x 0,871 * 32,066 u - = ----------------- y 55,847 u
Durch Vereinfachen und Ausrechnen erhält man:
x 1 - = 0,5 = - y 2
Da x die Anzahl der Eisenatome angibt und y die Anzahl der Schwefelatome, kennt man nun das Anzahlverhältnis der Atome in Pyrit:
N(Fe):N(S) = 1:2 auf ein Eisenatom kommen zwei Schwefelatome
Die Verhältnisformel für Pyrit gibt dieses Anzahlverhältnis an. Folglich lautet die Verhältnisformel für Pyrit:
FeS2 N(Fe):N(S) = 1:2
Darstellung einer Stoffportion Eisensulfid und einer Stoffportion Pyrit mithilfe des Teilchenmodells:
